1.) HIDROCABUROS
Los hidrocarburos son compuestos orgánicos formados únicamente por carbono e hidrógeno.
Consisten en un armazón de carbono al que se unen átomos de hidrógeno.Forman el esqueleto de la materia orgánica.
Clasificación
Según la estructura de los enlaces entre los átomos de carbono, se clasifican en:
Hidrocarburos acíclicos, alifáticos o de cadena abierta: estos a su vez se dividen en:
Hidrocarburos saturados (alcanos o parafinas), que no tienen enlaces dobles, triples, ni aromáticos.
Hidrocarburos insaturados, que tienen uno o más enlaces dobles (alquenos u olefinas) o triples (alquinos o acetilénicos) entre sus átomos de carbono;
Hidrocarburos cíclicos, que a su vez se subdividen en:
Hidrocarburos nafténicos, que tienen cadenas cerradas de 3, 4, 5, 6, 7 y 8 átomos de carbono saturados o no saturados.
Hidrocarburos aromáticos, no saturados, que poseen al menos un anillo aromático además de otros tipos de enlaces que puedan tener.
Los hidrocarburos extraídos directamente de formaciones geológicas en estado líquido se conocen comúnmente con el nombre de petróleo, mientras que a los que se encuentran en estado gaseoso se les conoce como gas natural.
Los hidrocarburos constituyen una actividad económica de primera importancia, pues forman parte de los principales combustibles fósiles (petróleo y gas natural), así como de todo tipo de plásticos, ceras y lubricantes.
Clases de formulas de los compuestos orgánicos:
Forma Desarrollada o estructural: Muestra la ubicación en el espacio de los átomos en la formula.
Forma Semidesarrollada o Semiestructurada: Muestra el tipo de enlace que hay entre los átomos de carbonos e hidrógenos.
Forma Global, general o empírica: Muestra la cantidad de los átomos de un carbono e hidrogeno en la formula.
Formula Funcional: Aquella que destaca el grupo funcional que se encuentra presente en el compuesto
1.) HIDROCABUROS
Los hidrocarburos son compuestos orgánicos formados únicamente por carbono e hidrógeno. Consisten en un armazón de carbono al que se unen átomos de hidrógeno. Forman el esqueleto de la materia orgánica.
Clasificación
Según la estructura de los enlaces entre los átomos de carbono, se clasifican en:
Hidrocarburos acíclicos, alifáticos o de cadena abierta: estos a su vez se dividen en:
Hidrocarburos saturados (alcanos o parafinas), que no tienen enlaces dobles, triples, ni aromáticos.
Hidrocarburos insaturados, que tienen uno o más enlaces dobles (alquenos u olefinas) o triples (alquinos o acetilénicos) entre sus átomos de carbono;
Hidrocarburos cíclicos, que a su vez se subdividen en:
Hidrocarburos nafténicos, que tienen cadenas cerradas de 3, 4, 5, 6, 7 y 8 átomos de carbono saturados o no saturados
Hidrocarburos aromáticos, no saturados, que poseen al menos un anillo aromático además de otros tipos de enlaces que puedan tener.
Los hidrocarburos extraídos directamente de formaciones geológicas en estado líquido se conocen comúnmente con el nombre de petróleo, mientras que a los que se encuentran en estado gaseoso se les conoce como gas natural. Los hidrocarburos constituyen una actividad económica de primera importancia, pues forman parte de los principales combustibles fósiles (petróleo y gas natural), así como de todo tipo de plásticos, ceras y lubricantes.
Clases de formulas de los compuestos orgánicos:
Forma Desarrollada o estructural: Muestra la ubicación en el espacio de los átomos en la formula.
Forma Semidesarrollada o Semiestructurada: Muestra el tipo de enlace que hay entre los átomos de carbonos e hidrógenos.
Forma Global, general o empírica: Muestra la cantidad de los átomos de un carbono e hidrogeno en la formula.
Formula Funcional: Aquella que destaca el grupo funcional que se encuentra presente en el compuesto
2.) FUNCIONES OXIGENADAS:
Alcoholes o Fenoles
Aldehídos
Cetonas
Éteres
Ácidos
Orgánicos
Ésteres
Sales
Orgánicas
3.) FUNCIONES NITROGENADAS:
Aminas
Amidas
Cianuros
Nitrilos
Aminoácidos
Aldehídos:
H
-
H - C - H
-
H
Al reemplazar 1 oxigeno por 2 hidrógenos la formula quedaría así
H
-
C = O
-
H
EJEMPLO:
1).-
H
-
H - C - H
-
H - C - H
-
H
Quedaría así:
H
-
C = O
-
C = O
-
H
2).-
H
-
H - C - H
-
H - C - H
-
H - C - H
-
H
Quedaría así:
H
-
C = O
-
H - C - H
-
C = O
-
H
OJO: 1 oxigeno reemplaza a m2 hidrogeno, pero tiene que ser un carbono primario y se forma un carbonilo, que es parte de los aldehidos.
CHO
-
CH2
-
CH3
CARBONILOS:
-BUTANAL
C3H7CHO
-EXANAL
C5H11CHO
-EXANAL
C5H9CHO
-TRIDECANO DIAL
C11H22 (CHO)2
-TRIDECA DIENO INO DIAL
C11H14 (CHO)2
REGLA PARA ESCRIBIR ALDEHIDOS EN
1).- Primero debe de escribir CH CHO
2).- Luego tienes que ver cuantos carbonos te piden
3).- El numero de carbonos se restan con el numero de carbonos en el carbonilo teniendo en cuenta que 1 oxigeno reduce 2 hirogenos.
4).- Veo si hay enlaces dobles o triples y la cantidad que me den lo resto con la cantidad obtenida de la resta de los carbonos obtenidos.
-DODECATRIENO INO AL
C11H13CHO
-OCTINODIAL
C6H8 CHO
-HEPTENO DIINO AL
C6H3 CHO
-DECATRIENO DIINO AL
C9H5 CHO
FORMULA SEMIDESARROLADA
-Hepteno3 diino 1-5 AL 7
C C – C = C – C C - CHO
-EXENO 2 AL1
CHO – C = C – C – C - C
-OCTINO 6 DIAL 1-8
CHO – C – C – C – C – C C - CHO
-DODECATRIENO 3-7-9 INO 5 AL 1
CHO – C – C = C – C C – C = C – C = C – C - C
-TRIDECADIENO 6 -9 INO 3 DIAL 1-13
CHO – C – C C – C – C = C – C – C = C – C – C – CHO
Cetonas
Es aquella funcion quimica en donde un oxigeno reeemplaza a 2 hidrogenos en un carbono secundario
ejemplo:
alcoholes
Son aquellos grupos donde se unen 1 hidrogeno y un oxigeno y se forman un oxidrilo.
ejemplos:
Eteres
Son aquellos que con la union de 2 hidrogenos y 1 oxigeno y forman una molecula de agua
ROH + HOR' → ROR' + H2O
ejemplo:
Correccion de la prueba número 1
heptadienil 4 - ciclopropil 2, Penteno 2
2.) Escribe la Fórmula Global de los siguientes compuestos:
3.) Escribe la Fórmula Global de un Hidrocarburo que tiene lo siguiente:
- 14 Carbonos
- 3 Enlaces Dobles (- 6H)
- 2 Enlaces Triples (- 8H)
- 2 Radicales :
SOLUCIÓN DE
1.- Escribe la formula semidesarrollada de los sgts compuestos
a) butinil 6 – reptil – ciclopentil 2, Noveno 4
H3C HC CH HC CH3 C4H5 CH2 CH CH C7H15 CH2
b) metil 5 – (trimetil 1-1-2, propil) 5, Undecatetraeno 1-3-5-9
No sale porque al carbono 5 le piden 5 enlaces y se sabe que cada carbono solo puede tener 4 enlaces o hidrógenos.
c) etil 2 – metil 5, exanodiol 1-5
OHH2C HC CH2 OHC CH3 CH3 C2H5 CH2
d) bromo 2- pentil 4 –ciclopropil 7, Decadieno 3-9 diol 1,6
OHH2C HCBr CH H2C C C5H11 C OH H CH C3H5 CH2 CH CH2
2.- Escribe la fórmula funcional
· C16
· 3 = à - 6 Hidrógenos
· 2 ≡ à - 8 Hidrógenos
· 2 I à - 2 Hidrógenos
·
·
· octeninil à C8H11
· decil à C10H21
- 3 Hidrógenos
· triol à - 3 Hidrógenos
- 25 Hidrógenos
C16H34 – 25 = 8
C16H12 C41H59I2CL3 (OH)3
C7H15
C8H11
C10H21
C41H59
Aldehidas:
Los aldehídos son compuestos orgánicos caracterizados por poseer el grupo funcional -CHO:
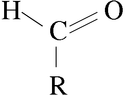 Es decir, el grupo carbonilo -C = O está unido a un solo radical orgánico.
Es decir, el grupo carbonilo -C = O está unido a un solo radical orgánico.
Se nombran sustituyendo la terminación -o del nombre del hidrocarburo por -al. Los aldehídos más simples (metanal y etanal) tienen otros nombres que no siguen el estándar de
Los nombres de los aldehídos, se obtienen cambiando la terminación -ol del alcohol del cual proviene por la terminación al.
Por ejemplo:
- CH3-CH2-OH Etanol, Alcohol
- CH3-CH=O Etanal, Aldehído
Cetonas:
Una cetona es un compuesto que contiene el grupo carbonilo. Cuando el grupo funcional carbonilo es el más importante del compuesto orgánico, las cetonas se nombran agregando el sufijo -ona al hidrocarburo del cual provienen (hexano, hexanona; heptano, heptanona; etc). También se puede nombrar anteponiendo cetona a los radicales a los cuales está unido. Cuando el grupo carbonilo no es el grupo prioritario, se utiliza el prefijo oxi- (ejemplo: 2-oxopropanal).
El grupo funcional carbonilo es un átomo de carbono unido con un doble enlace a un átomo de oxígeno, y además unido a otros dós átomos de carbono.
El tener dos átomos de carbono unidos al grupo carbonilo, es lo que lo diferencia de los ácidos carboxílicos, aldehídos, ésteres. El doble enlace con el oxígeno, es lo que lo diferencia de los alcoholes y éteres. Las cetonas suelen ser menos reactivas que los aldehídos dado que los grupos alquílicos actúan como dadores de electrones por efecto inductivo.



